Règles UICPA de nomenclature
Nomenclature des composés acycliques
Étape 1 : Déterminer le groupe fonctionnel principal
a) Déterminer le groupe fonctionnel principal de la molécule
| Ex. |

|
suffixe : -ane |
La molécule ne contient que les liaisons carbone-carbone et carbone-hydrogène donc il n’y a pas de groupe fonctionnel. Cette molécule est alors un alcane et aura le suffixe –ane.
b) Lorsqu’une molécule contient plus qu’un groupe fonctionnel, le groupe principal est celui avec la plus haute priorité (voir annexe I). Dans l’Ex ci-dessous, il est représenté en rouge. Ce groupe principal est utilisé afin de déterminer le suffixe du nom. Les autres groupes fonctionnels (si applicable) sont mis en préfixe.
| Ex. |

|
suffixe : -al préfixe : hydroxy- |
La molécule contient deux groupes fonctionnels, un aldéhyde (en rouge) et un alcool (en bleu). L’aldéhyde est de plus haute priorité donc il est le groupe fonctionnel principal et détermine alors que le suffixe du nom sera –al. Puisque l’alcool est moins prioritaire on accorde le préfixe hydroxy- au nom de la molécule.
c) Les alcènes et alcynes ne sont jamais mis en préfixe, ils sont toujours en suffixe. Donc, s’il y a un groupe fonctionnel avec une plus haute priorité, mettre l’alcène et l’alcyne en suffixe entre la racine du nom et le suffixe du groupe fonctionnel principal (-èn- au lieu de –ène et -yn- au lieu de –yne).
| Ex. |
|
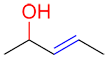
L’alcool (en rouge) est le groupe fonctionnel principal de cette molécule donc on utilise le suffixe –ol. Puisque l’alcène (en bleu) n’est pas prioritaire mais qu’il est toujours en suffixe, on accorde le suffixe –ènol au nom de la molécule.
Étape 2 : Déterminer la chaine principale de carbone
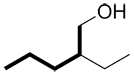
a) La plus longue chaine contenant le groupe fonctionnel principal
| Ex. |
|
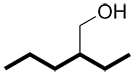
au lieu de |
|
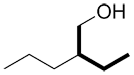
ou |
|
b) Si plus d’un choix est possible, choisir la chaine avec le nombre maximal de liaisons multiples
| Ex. |

|
au lieu de |

|
ou |

|
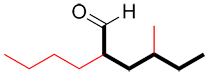
c) Si deux chaines de la même longueur sont possibles, choisir la chaine avec le nombre maximal de substituants
| Ex. |
|
au lieu de |

|
| 2 substituants | 1 substituants |
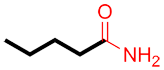
Étape 3 : Nommer la chaine principale
Nommer la chaine principale ainsi que le groupe principal. Donner à la chaine principale le même nom que si c’était un alcane (voir annexe III) mais en remplaçant la terminaison –ane par le suffixe caractéristique du groupe fonctionnel prioritaire.
| Ex. |
|
|
Étape 4 : Numéroter la chaine principale
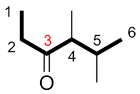
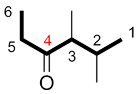
a) Numéroter tous les carbones de la chaine principale consécutivement afin que le groupe fonctionnel principal ait le plus petit indice possible
| Ex. |
|
au lieu de |
|
b) Si le même indice est obtenu pour le groupe principal en numérotant dans les deux directions, numéroter la chaine de façon à ce que les autres substituants aient le plus petit indice possible
| Ex. |

|
au lieu de |
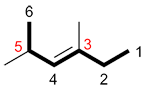
|
| Ex. |

|
au lieu de |
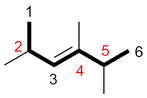
|
c) Si les indices pour les substituants sont pareils en numérotant dans les deux directions, attribuer le plus petit indice au premier substituant en ordre alphabétique
| Ex. |
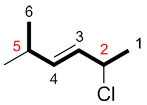
|
au lieu de |
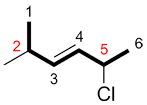
|
| «2-chloro…» | «2-méthyl…» |
Étape 5 : Indiquer la position du groupe fonctionnel principal
Indiquer la position du groupe fonctionnel principal dans le nom, entre la racine et le suffixe correspondant au groupe principal (voir section «à noter» pour les exceptions).
| Ex. |

|
|
Étape 6 : Nommer les substituants
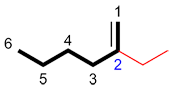
Nommer les groupements alkyls, halogènes et autres substituants, et déterminer leur position(s) sur la chaine principale grâce à la numérotation établie lors de l’étape 4. Les alkyls sont les dérivés des alcanes (un alcane qui a perdu un hydrogène). Pour les nommer, utiliser la racine du nom de l’alcane (désigné par le nombre de carbones) et ajouter la terminaison –yl. Donc une rammification de 1 carbone sur une chaine principale se nomme «méthyl».
| Ex. |
|
|
Pour le substituant on obtient alors le nom «2-éthyl»
Cette logique s’applique aussi pour les alkoxy (éthers). Les éthers ont la formule –OR, dont le R du groupement -OR est l’alkyl. Nommer le comme mentionné ci-dessus et au lieu d’ajouter la terminaison –yl, on ajoute –oxy.
Étape 7 : Assigner la stéréochimie
Assigner la stéréochimie aux centres chiraux (voir annexe VI) et aux liaisons doubles (voir annexe V):
a) Les alcènes di-substitués peuvent être nommés selon la nomenclature cis/trans ou selon la nomenclature E/Z. La nomenclature E/Z est préférée.
| Ex. |

|
et |

|
| (E) ou trans | (Z) ou cis |
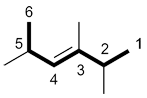
b) Les alcènes tri- et tétra-substitués ne peuvent être nommés qu’avec la nomenclature E/Z.
| Ex. |
|
(E) |
c) Les atomes des carbones chiraux sont assignés une configuration (R) ou (S).
| Ex. |

|
et |

|
| (S) | (2S,3R) |
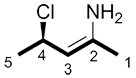
d) Lorsque la nomenclature (R/S) et (E/Z) est présente, elle est assignée entre parenthèses, en italique lorsque tapé et avec les indices en ordre croissant. Les parenthèses sont suivies d’un trait d’union avant le début du nom.
| Ex. |
|
(2Z,4R)- |
Étape 8 : Construire le nom complet
Écrire le nom au complet en 1 mot en incluant les indices pour les substituants, énumérés en ordre alphabétique. N’oubliez pas d’inclure la stéréochimie lorsqu’applicable.
a) Inclure les préfixes multiplicatifs (voir annexe IV.) pour des substituants identiques. Par contre ils n’ont pas d’effet sur l’ordre alphabétique des substituants.
b) Séparer les indices indiquant la position des substituants par des virgules
c) Rejoindre les lettres du nom aux indices par des traits d’union
d) Noter que l'accent è pour l'alcène devient un é dans le nom au complet
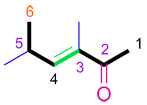
Nomenclature UICPA complète :
|
|
| (E)-3,5-diméthylhex-3-én-2-one |
Nomenclature des composés cycliques
Étape 1 : Déterminer le groupe fonctionnel principal
a) Déterminer le groupe fonctionnel principal de la molécule
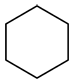
| Ex. |
|
suffixe : -ane |
La molécule ne contient que les liaisons carbone-carbone et carbone-hydrogène donc il n’y a pas de groupe fonctionnel. Cette molécule est alors un alcane et aura le suffixe –ane.
b) Lorsqu’une molécule contient plus qu’un groupe fonctionnel, le groupe principal est celui avec la plus haute priorité (voir annexe I). Dans l’Ex ci-dessous, il est représenté en rouge. Ce groupe principal est utilisé afin de déterminer le suffixe du nom. Les autres groupes fonctionnels (si applicable) sont mis en préfixe.
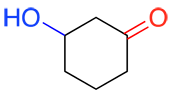
| Ex. |
|
suffixe : -one préfixe : hydroxy- |
La molécule contient deux groupes fonctionnels, un aldéhyde (en rouge) et un alcool (en bleu). L’aldéhyde est de plus haute priorité donc il est le groupe fonctionnel principal et détermine alors que le suffixe du nom sera –al. Puisque l’alcool est moins prioritaire on accorde le préfixe hydroxy- au nom de la molécule.
c) Les alcènes et alcynes ne sont jamais mis en préfixe, ils sont toujours en suffixe. Donc, s’il y a un groupe fonctionnel avec une plus haute priorité, mettre l’alcène et l’alcyne en suffixe entre la racine du nom et le suffixe du groupe fonctionnel principal (-èn- au lieu de –ène et -yn- au lieu de –yne).
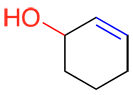
| Ex. |
|
L’alcool (en rouge) est le groupe fonctionnel principal de cette molécule donc on utilise le suffixe –ol. Puisque l’alcène (en bleu) n’est pas prioritaire mais qu’il est toujours en suffixe, on accorde le suffixe –ènol au nom de la molécule.
Étape 2 : Déterminer la chaine principale de carbone
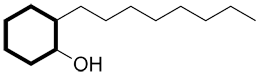
Lorsque le groupe fonctionnel principal est sur un cycle, identifier le cycle comme la chaine principale.
| Ex. |
|
au lieu de |

|
| Ex. |
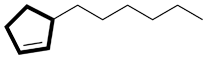
|
au lieu de |
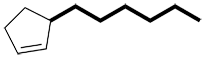
|
Étape 3 : Nommer la chaine principale
Nommer la chaine principale ainsi que le groupe principal. Donner à la chaine principale le même nom que si c’était un alcane (voir annexe III) mais en remplaçant la terminaison –ane par le suffixe caractéristique du groupe fonctionnel prioritaire. Ajouter le préfixe cyclo- au nom.
| Ex. |
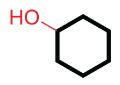
|
|
| cyclohexanol |
Étape 4 : Numéroter la chaine principale
a) Lorsque les composés cycliques sont monosubstitués, le carbone auquel le substituant principal est lié est toujours C1. Cet indice n’est pas nécessaire dans le nom chez les cycles monosubstitués.
| Ex. |

|
cyclopentanol |
b) Chez les composés cycliques polysubstitués, le point de départ et la direction de la numérotation est déterminé en s’assurant que le plus petit indice possible est attribué aux facteurs suivants en ordre consécutif :
i. Le carbone auquel le groupe fonctionnel principal est lié est le C1 et la numérotation continue dans le sens qui permet les plus petits indices possibles aux substituants
| Ex. |
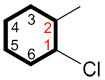
|
au lieu de |

|
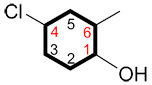
et |
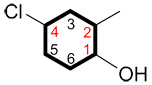
|
au lieu de |
|
ii. Lorsqu’on nomme un cycloalcène et que l’alcène est le groupe fonctionnel principal on lui attribue l’indice 1, mais il n’est pas nécessaire de l’inclure dans le nom.
| Ex. |

|
5-chloro-3-méthylcyclohexène |
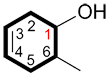
iii. Lorsqu’un groupe fonctionnel de plus haute priorité est présent, le carbone lié au groupe devient C1 et la numérotation se fait dans le sens attribuant le plus petit indice possible à l’alcène.
| Ex. |
|
6-méthylcyclohex-3-ènol |
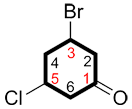
iv. Si on obtient les mêmes indices dans les deux sens, on attribue le plus petit indice au substituant qui est nommé en premier (ordre alphabétique).
| Ex. |
|
au lieu de |
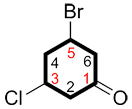
|
| 3-bromo-5-chlorocyclohexanone | 5-bromo-3-chlorocyclohexanone |
Étape 5 : Indiquer la position du groupe fonctionnel principal
Le groupe fonctionnel prioritaire doit toujours être sûre le C1, il n'est donc pas nécessaire d'indiquer cette position dans le nom. Par contre, s'il y a d'autres groupes fonctionnels présents, en préfixe ou en suffixe, leur positions doivent être indiquées.
Étape 6 : Nommer les substituants
Nommer les groupements alkyls, halogènes et autres substituants, et déterminer leur position(s) sur la chaine principale grâce à la numérotation établie lors de l’étape 4. Les alkyls sont les dérivés des alcanes (un alcane qui a perdu un hydrogène). Pour les nommer, utiliser la racine du nom de l’alcane (désigné par le nombre de carbones) et ajouter la terminaison –yl. Donc une rammification de 1 carbone sur une chaine principale se nomme «méthyl». Pour plus de détails, veuillez voir l’étape 6 des composés acycliques.
| Ex. |
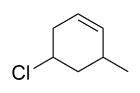
|
5-chloro-3-méthylcyclohexène |
Étape 7 : Assigner la stéréochimie
Assigner la stéréochimie aux centres chiraux :
Les cycloalcanes substitués peuvent être nommés selon la nomenclature cis/trans ou (R/S), mais la nomenclature (R/S) est plus précise et devrait être utilisée lorsque possible.
| Ex. |
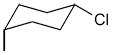
|
et |
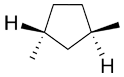
|
| cis (R/S pas applicable ici) |
trans ou (R,R) Ici (R,R) est plus précis car (S,S) serait trans aussi. |
Étape 8 : Construire le nom complet
Écrire le nom au complet en 1 mot en incluant les indices pour les substituants, énumérés en ordre alphabétique. N’oubliez pas d’inclure la stéréochimie lorsqu’applicable.
a) Inclure les préfixes multiplicatifs (voir annexe IV.) pour des substituants identiques. Par contre, ils n’ont pas d’effet sur l’ordre alphabétique des substituants.
b) Séparer les indices indiquant la position des substituants par des virgules
c) Rejoindre les lettres du nom aux indices par des traits d’union
d) Noter que l'accent è pour l'alcène devient un é dans le nom au complet
Nomenclature UICPA complète :
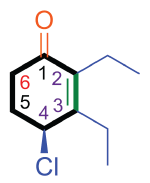
|
|
| (S)-4-chloro-2,3-diéthylcyclohex-2-énone |
Nomenclature des dérivés de benzène
En général
En général on nomme les dérivés de benzène (le cyclohexa-1,3,5-triène) comme les autres composés cycliques sauf que la racine devient «benzène» ou lieu de «cycloalcane» ou «cycloalcène».
| Ex. |
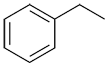
|
éthylbenzène |
2 substituants
Lorsqu’un dérivé de benzène a deux substituants, on peut utiliser la nomenclature ortho (o), méta (m) et para (p) afin de désigner la position des substituants.
| Ex. |
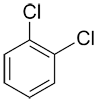
|
o-dichlorobenzène ou 1,2-dichlorobenzène |
| Ex. |
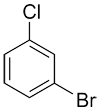
|
m-bromochlorobenzène ou 1-bromo-3-chlorobenzène |
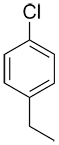
| Ex. |
|
p-chloroéthylbenzène ou 1-chloro-4-éthylbenzène |
>2 substituants
Lorsque le dérivé de benzène a plus de deux substituants, on indique la position de tous les substituants selon les indices attribués par la numérotation. Notez qu'on alphabétise les substituants.
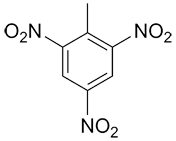
| Ex. |
|
1-méthyl-2,4,6-trinitrobenzène ou 2,4,6-trinitrotoluène |
Nom communs
Certains noms communs sont acceptés et couramment utilisés au lieu du nom selon l’Union international en chimie pure et appliquée (l’UICPA)
| Ex. |

|

|
|
|
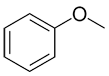
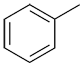
| Commun : | phénol | aniline | anisole | toluène |
| UICPA : | benzènol | benzènamine | méthoxybenzène | méthylbenzène |
| Autres noms acceptés : | hydroxybenzène | aminobenzène | phénoxyméthane | phénylméthane |
À noter
Les exceptions à l'étape 5
Ne pas indiquer la position du groupe fonctionnel principal lorsqu’il ne peut être lié qu’au carbone 1, donc en position terminale. Ceci est le cas pour les acides carboxyliques, les esters, les amides et les aldéhydes. Aussi, ne pas indiquer la position lorsqu’une seule position est possible.
| Ex. |

|
et |

|
| butanone | propanone |
Les substituants complexes
Un substituant complexe est nommé en suivant les mêmes étapes tout comme s’il était une molécule indépendante. La numérotation des indices commence au carbone qui est lié à la chaine principale, ensuite on donne au substituant le suffixe –yl et ce nom est présenté en parenthèses dans le nom complet de la molécule.
| Ex. |

|
| 3-(4-hydroxycyclohexyl)-propane-1,2-diol |
Annexes
Annexe I : La priorité des groupes fonctionnels (abrégé)
| Groupe fonctionnel | Formule | Suffixe (lorsque prioritaire) | Préfixe (lorsque secondaire) | |
|---|---|---|---|---|
|
Acide carboxylique |

|
acide -oïque | carboxy- |
| Ester |

|
(R) -oate | (R)-oxycarbonyl | |
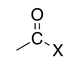
| Halogénure d’acyle |
|
halogénure -oyle | halocarbonyl- | |
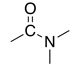
| Amide |
|
-amide | carbamoyl- | |
| Nitrile |

|
-nitrile | cyano- | |
| Aldéhyde |

|
-al | oxo- | |
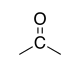
| Cétone |
|
-one | oxo- | |
| Alcool |
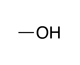
|
-ol | hydroxy- | |
| Thiol |
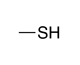
|
-thiol | sulfanyl- | |
| Amine |

|
-amine | amino- | |
| Imine |
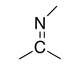
|
-imine | (R)-imino | |
| Éther |

|
— | (R)-oxy- | |
| Sulfide |
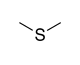
|
— | (R)-sulfanyl | |
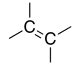
| Alcène |
|
-ène | — | |
| Alcyne |
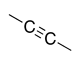
|
-yne | — | |
| Halogénures d’alkyle |

|
— | *halo- | |
| Nitré |

|
— | nitro- |
* Br: bromo, Cl: chloro, F: fluoro, I: iodo
Annexe II : Les alcanes non ramifiés
| Nombre de carbones | Nom | Nombre de carbones | Nom |
|---|---|---|---|
| 1 | Méthane | 11 | Undécane |
| 2 | Éthane | 12 | Dodécane |
| 3 | Propane | 13 | Tridécane |
| 4 | Butane | 14 | Tétradécane |
| 5 | Pentane | 15 | Pentadécane |
| 6 | Hexane | 16 | Hexadécane |
| 7 | Heptane | 17 | Heptadécane |
| 8 | Octane | 18 | Octadécane |
| 9 | Nonane | 19 | Nonadécane |
| 10 | Décane | 20 | Eicosane |
Annexe III : Les préfixes multiplicatifs
| Nombre de substituants identiques | Préfixe |
|---|---|
| 2 | di |
| 3 | tri |
| 4 | tétra |
Annexe IV : La nomenclature E/Z
En plus de la nomenclature cis/trans, la nomenclature E/Z peut être utilisée lorsqu’un alcène est di-substitué mais la nomenclature E/Z est toujours préférable car elle est plus précise et peut être utilisée peut importe si un alcène est di-, tri- ou tétra-substitué.
Le «Z» vient du mot allemand «zusammen» qui signifie «ensemble» et le «E» vient du mot allemand «entgegen» qui signifie «opposé».
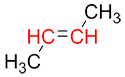
Cette nomenclature est appliquée en examinant les substituants des deux carbones de l’alcène (les carbones représentés en rouge dans l’Ex ci-dessous).
| Ex. |
|
Étape 1 :
En premier, trouver le substituant prioritaire des deux carbones de l’alcène (c’est-à-dire le premier atome du substituant avec le numéro atomique le plus élevé).
| Ex. |
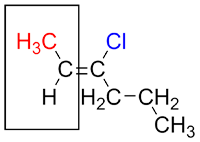
|
Comparer le groupement méthyl avec le H sur le carbone à gauche. Le substituant prioritaire est le méthyl, puisque le carbone a un numéro atomique plus élevé que H.
| Ex. |

|
Comparer le groupement propyl avec le chlore. Le substituant prioritaire est le chlore, puisque le chlore a un numéro atomique plus élevé que le carbone.
Étape 2 :
Comparer la position des deux substituants prioritaires.
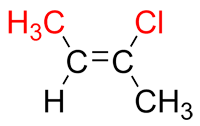
S’ils sont du même côté de la liaison double, donc «ensemble», désigner l’alcène (Z).
| Ex. |
|
S’ils sont de différents côtés de la liaison double, donc «opposés», désigner l’alcène (E)
| Ex. |

|
Annexe V : La nomenclature R/S
La nomenclature R/S est utilisée afin de distinguer des énantiomères, soit des isomères dont la configuration (l’arrangement spatial) est différente. Ces isomères ont un atome, typiquement un carbone, asymétrique (un atome lié a 4 différents substituants). Le «R» et «S» sont dérivés des mots latins «rectus» et «sinistra» qui signifient «droite» et «gauche» respectivement.
| Ex. |
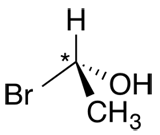
|
Un carbone chiral (*) signifie que c’est un carbone asymétrique
Étape 1 :
a) Assigner la priorité (de 1 à 4 où 1 est prioritaire) aux quatre substituants du carbone asymétrique. La priorité est assignée selon l’atome avec le numéro atomique le plus élevé.
| Ex. |
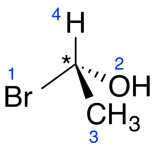
|
|
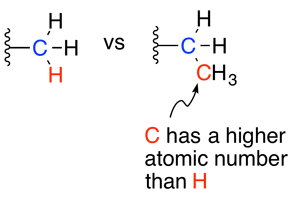
b) Lorsque la priorité ne peut pas être déterminée à partir des numéros atomiques des atomes directement liés aux carbone asymétrique (partie a), continuer ce même processus avec la deuxième série d’atomes des substituants sans priorité assignée jusqu'à ce qu’il y ait une différence.
| Ex. |
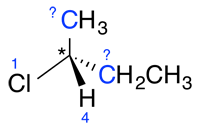
|
|
|
|
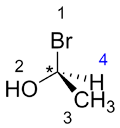
Étape 2 :
Faire une rotation de la molécule pour que le substituant le moins prioritaire (4) soit en arrière de la molécule.
| Ex. |

|
à |
|
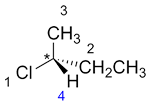
| Ex. |
|
à |

|
Étape 3 :
Tracer une trajectoire de 1 – 2 – 3. Si la trajectoire va dans le sens des aiguilles d’une montre, désigner la molécule (R)
| Ex. |

|
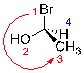
Si la trajectoire va dans le sens contraire des aiguilles d’une montre, désigner la molécule (S)
| Ex. |
|

|
Annexe VI : Autres noms communs acceptés
Lorsqu’on nomme des alcanes, p.ex. pentane, il est sous-entendu qu’on fait référence à la forme non ramifiée de la molécule. Utiliser le «n» (en italique lorsque tapé) suivit d’un trait d’union devant le nom afin de préciser que c’est la forme linéaire (p.ex. n-pentane) et non un des isomères de constitution.
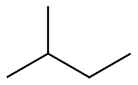
Ex : Le 2-méthylbutane et le 2,2-diméthylpropane sont des isomères de consitution du pentane car ils ont chacun 5 carbones. Ils sont aussi communément nommés isopentane et néopentane, respectivement.

|
|

|
| n-pentane | 2-méthylbutane | 2,2-diméthylpropane |
| (pentane) | (isopentane) | (néopentane) |
Chez les alcanes, il y a aussi certains noms communs acceptés pour identifier des ramifications (des groupements alkyl).
| isopropyl = 1-méthyléthyl |

|
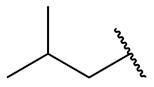
| isobutyl = 2-méthylpropyl |
|
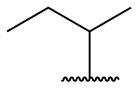
| sec-butyl = 1-méthylpropyl |
|
| tert-butyl = 1,1-diméthyléthyl |

|
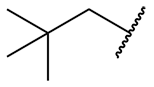
| néopentyl = 2,2-diméthylpropyl |
|
Seulement les préfixes suivis d’un trait d’union n’ont pas d’effet sur l’ordre alphabétique des substituants. Les abréviations s- (pour sec-) et t- (pour tert-) sont aussi acceptées.



